2021年6月22日�,藥監總局發布醫療器械優先審批申請審核結果公示(2021年第9號)����,胚胎植入前染色體非整倍體檢測試劑盒(半導體測序法)因為產品屬于列入國家重點研發計劃的醫療器械����,通過醫療器械優先審批。詳見正文�。
引言:2021年6月22日�,藥監總局發布醫療器械優先審批申請審核結果公示(2021年第9號)�����,胚胎植入前染色體非整倍體檢測試劑盒(半導體測序法)因為產品屬于列入國家重點研發計劃的醫療器械�����,通過醫療器械優先審批。詳見正文����。
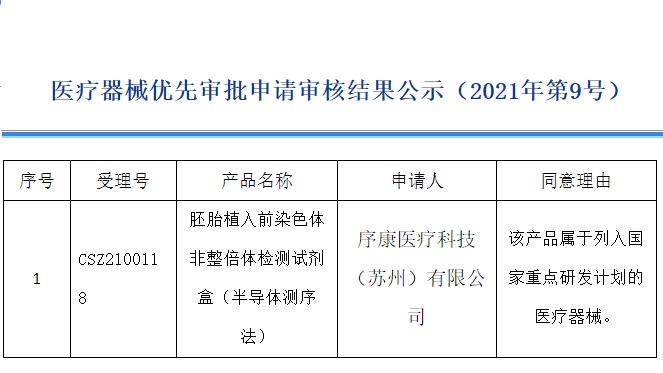
依據原國家食品藥品監督管理總局《醫療器械優先審批程序》(總局公告2016年168號)�,我中心對申請優先審批的醫療器械注冊申請進行了審核。下述項目符合優先審批情形����,擬定予以優先審批����,現予以公示�����。
序號 | 受理號 | 產品名稱 | 申請人 | 同意理由 |
1 | CSZ2100118 | 胚胎植入前染色體非整倍體檢測試劑盒(半導體測序法) | 序康醫療科技(蘇州)有限公司 | 該產品屬于列入國家重點研發計劃的醫療器械����。 |
公示時間:2021年6月22日至2021年6月29日
公示期內����,任何單位和個人有異議的����,可以填寫醫療器械優先審批項目異議表,書面提交至我中心綜合業務部。����。
聯 系 人:李文霞
電話:010-86452913
地址:北京市海淀區氣象路50號院1號樓
國家藥品監督管理局
醫療器械技術審評中心
2021年6月22日