2021年11月9日,國家藥品監督管理局醫療器械標準管理中心對外發布關于征求《醫療器械分類目錄》(調整意見)的通知。《醫療器械分類目錄》(調整意見)擬對部分醫美產品醫療器械分類做出調整。
2021年11月9日,國家藥品監督管理局醫療器械標準管理中心對外發布關于征求《醫療器械分類目錄》(調整意見)的通知。《醫療器械分類目錄》(調整意見)擬對部分醫美產品醫療器械分類做出調整。
11月9日消息,國家藥品監督管理局醫療器械標準管理中心對外發布關于征求《醫療器械分類目錄》(調整意見)的通知。
據悉,此次發布的《醫療器械分類目錄》(調整意見)系根據《醫療器械分類目錄動態調整工作程序》及相關要求,國家藥品監督管理局醫療器械標準管理中心組織醫療器械分類技術委員會專業組研究并形成。
其中,值得關注的是,《醫療器械分類目錄》(調整意見)擬對部分醫美產品監管類別做出調整,具體如下:
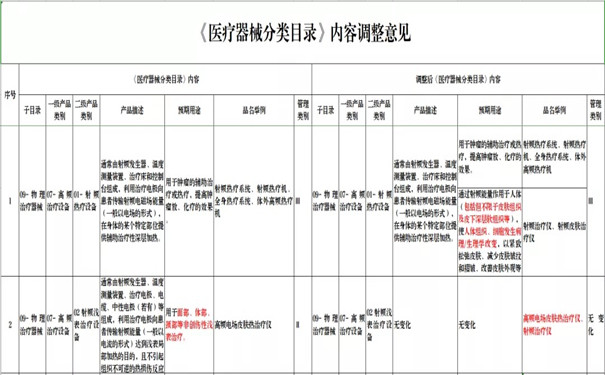
1、射頻治療儀、射頻皮膚治療儀,若產品通過射頻能量作用于人體(包括但不限于皮膚組織及皮下深層軟組織等),使人體組織、細胞發生病理/生理學改變,以緊致松弛皮膚、減少皮膚皺紋和褶皺、改善皮膚外觀等,擬按照III類器械監管。子目錄為09-物理治療器械,一級產品類別為07-高頻治療設備,二級產品類別為01-射頻熱療設備;(推薦閱讀:注意了 | 射頻美容類器械產品監管類別可能要調整!)
2、高頻電場皮膚熱治療儀、射頻治療儀,若產品用于面部、體部、頸部等非創傷性淺表治療,擬按照II類器械監管。子目錄為09-物理治療器械,一級產品類別為07-高頻治療設備,二級產品類別為02 射頻淺表治療設備;(推薦閱讀:注意了 | 射頻美容類器械產品監管類別可能要調整!)
3、新增面部埋植線品名舉例,擬按照III類器械監管。子目錄為13-無源植入器械,09-整形及普通外科植入物,二級產品類別為01-整形填充材料;
4、注射用透明質酸鈉溶液,由注射器以及預裝在注射器中的填充材料(一般以透明質酸鈉為主要成分)組成,產品用于注射至面部真皮層,主要通過所含透明質酸鈉等材料的保濕、補水等作用,改善皮膚狀態,擬按照III類器械監管。子目錄為13-無源植入器械,09-整形及普通外科植入物,二級產品類別為02整形用注射填充物