需進行醫療器械臨床試驗審批的第三類醫療器械目錄征求意見中
發布日期:2020-06-25 15:48瀏覽次數:2825次
近日�,國家藥監局綜合司發布《需進行臨床試驗審批的第三類醫療器械目錄(2020年修訂版�,征求意見稿)》�����,就需進行醫療器械臨床試驗審批產品目錄公開征求意見�����。
引言:近日,國家藥監局綜合司發布《需進行臨床試驗審批的第三類醫療器械目錄(2020年修訂版����,征求意見稿)》����,就需進行醫療器械臨床試驗審批產品目錄公開征求意見����。

國家藥監局綜合司公開征求《需進行臨床試驗審批的第三類醫療器械目錄(2020年修訂版����,征求意見稿)》意見
為進一步加強醫療器械臨床試驗的管理,維護醫療器械臨床試驗過程中受試者權益����,推進監管科學研究成果轉化�,提高審批效率�����,加快產品上市�,國家藥品監督管理局組織對需進行臨床試驗審批的第三類醫療器械目錄進行了修訂,起草了《需進行臨床試驗審批的第三類醫療器械目錄(2020年修訂版�����,征求意見稿)》(見附件)�����,現向社會公開征求意見����。請于2020年7月31日前����,將意見或建議以電子郵件方式反饋至ylqxzc@sina.cn,郵件主題請注明“需臨床試驗審批醫療器械目錄反饋意見”����。
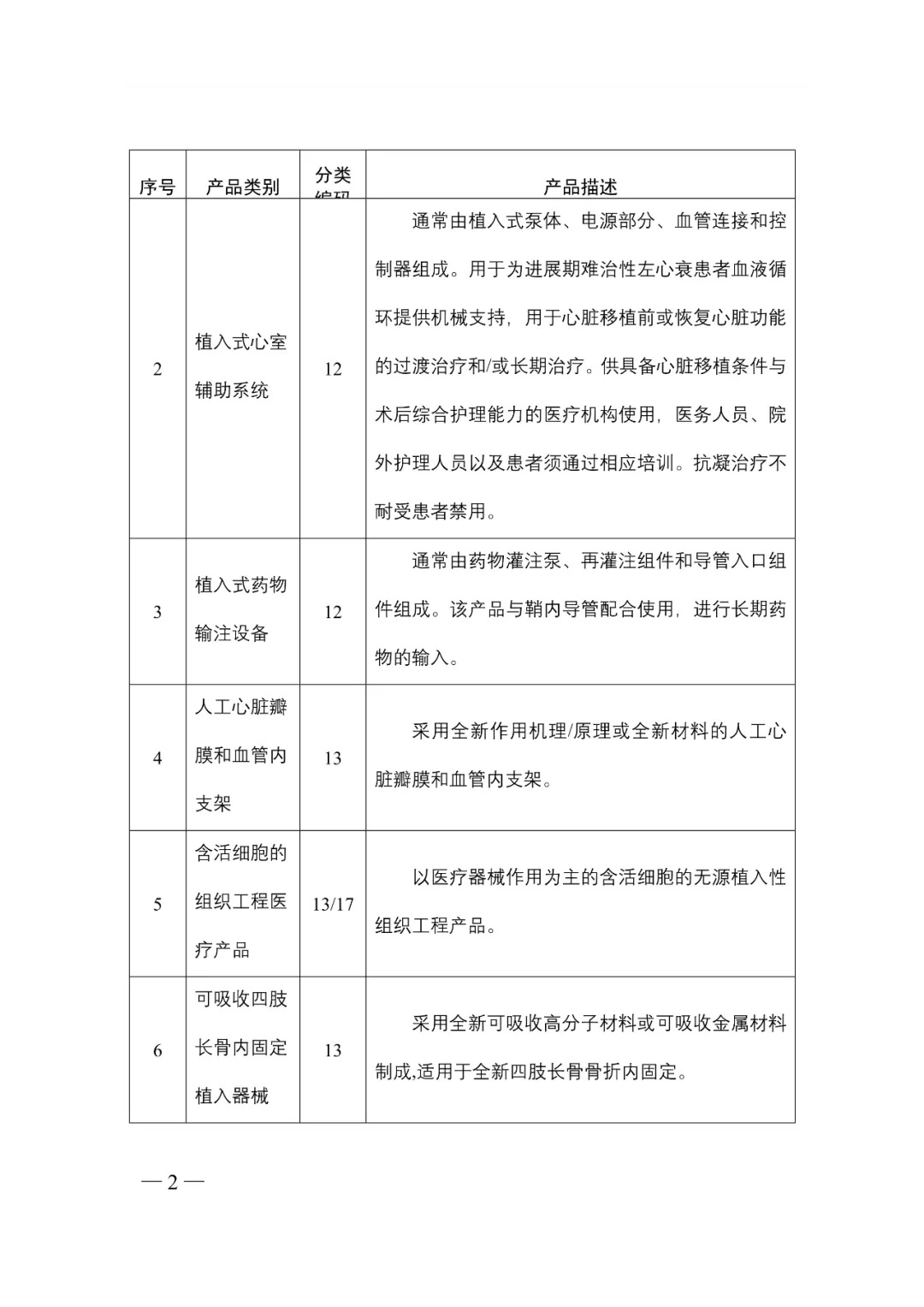
附件:需進行臨床試驗審批的第三類醫療器械目錄(2020年修訂版�,征求意見稿)
國家藥監局綜合司
2020年6月19日