歐盟的Basic-UDI是歐盟醫療器械CE認證法規中的一個概念,Basic UDI-DI跟著文件走,體現在證書、符合性聲明和技術文件中,實現的是文件對應的產品組的識別。Basic UDI-DI的要求已經于2021年5月26日開始生效,廣大制造商需要盡快申請編碼并納入自身的MDR文件體系。
一、Basic-UDI的組成和結構:
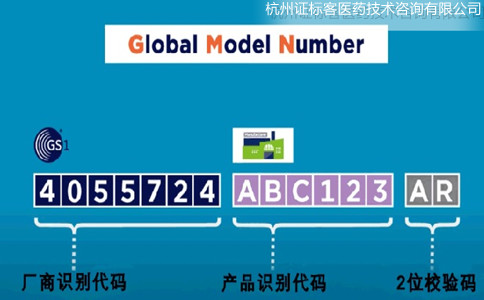
Basic UDI-DI是由Company Prefix + Model Reference+校驗碼組成,長度不能超過25位。其中,Company Prefix即廠商識別代碼,與UDI中的一致。Model Reference,也就是產品識別代碼,是由企業自行編制的,可以是字母+數字的形式。
二、什么地方用到Basic-UDI?
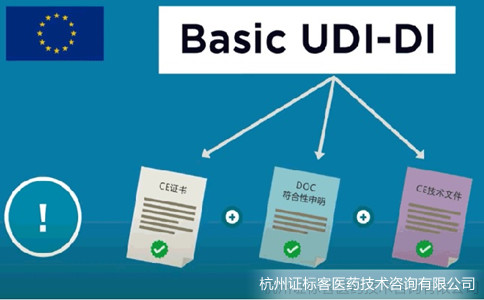
Basic UDI-DI是EUDAMED數據庫中關鍵信息,同時會體現在CE證書、歐盟符合性聲明和技術文件中。
寫這個有關歐盟Basic-UDI簡介,是希望大家能更早應對出口要求變化,更多疑問,歡迎您隨時方便與杭州證標客聯系。