2024年10月18日,國家藥監(jiān)局發(fā)布眼用透明質(zhì)酸鈉、膝關節(jié)翻修假體、醫(yī)用血管造影X射線系統(tǒng)、自動加樣系統(tǒng)、合成可吸收性外科縫線5個進口醫(yī)療器械注冊產(chǎn)品召回,一起來看具體情況。
2024年10月18日,國家藥監(jiān)局發(fā)布眼用透明質(zhì)酸鈉、膝關節(jié)翻修假體、醫(yī)用血管造影X射線系統(tǒng)、自動加樣系統(tǒng)、合成可吸收性外科縫線5個進口醫(yī)療器械注冊產(chǎn)品召回,一起來看具體情況。
一、愛惜康有限責任公司Ethicon LLC對合成可吸收性外科縫線主動召回
強生(上海)醫(yī)療器材有限公司報告,由于物料混淆導致部分包裝包含了錯誤的縫針型號和縫線規(guī)格,生產(chǎn)商愛惜康有限責任公司Ethicon LLC對其生產(chǎn)的合成可吸收性外科縫線MONOCRYL (Poliglecaprone 25) Monofilament Synthetic Absorbable Suture(國械注進20193022157)主動召回。召回級別為二級召回。本次召回涉及產(chǎn)品未進口至中國,具體型號、規(guī)格及批次等詳細信息見《醫(yī)療器械召回事件報告表》。

二、貝克曼庫爾特(美國)股份有限公司Beckman Coulter, Inc. 對自動加樣系統(tǒng)主動召回
貝克曼庫爾特國際貿(mào)易(上海)有限公司報告,由于軟件缺陷原因,生產(chǎn)商貝克曼庫爾特(美國)股份有限公司Beckman Coulter, Inc.對其生產(chǎn)的自動加樣系統(tǒng)CellMek SPS(國械備20230484)主動召回。召回級別為三級召回。本次召回涉及產(chǎn)品未進口至中國,具體型號、規(guī)格及批次等詳細信息見《醫(yī)療器械召回事件報告表》。

三、飛利浦醫(yī)療系統(tǒng)荷蘭有限公司Philips Medical Systems Nederland B.V對醫(yī)用血管造影X射線系統(tǒng)等產(chǎn)品主動召回
飛利浦(中國)投資有限公司報告,由于發(fā)現(xiàn)產(chǎn)品使用說明書和技術文檔的技術數(shù)據(jù)不一致,生產(chǎn)商飛利浦醫(yī)療系統(tǒng)荷蘭有限公司Philips Medical Systems Nederland B.V對其生產(chǎn)的醫(yī)用血管造影X射線系統(tǒng)Medical Angiography X-ray System(國械注進20203060323、國械注進20193060314、國械注進20193060315、國械注進20193060317、國械注進20193060319、國械注進20203060268、國械注進20223060150、國械注進20223060257)主動召回。召回級別為三級召回。本次召回涉及產(chǎn)品未進口至中國,具體產(chǎn)品的型號、規(guī)格及批次等詳細信息見《醫(yī)療器械召回事件報告表》。

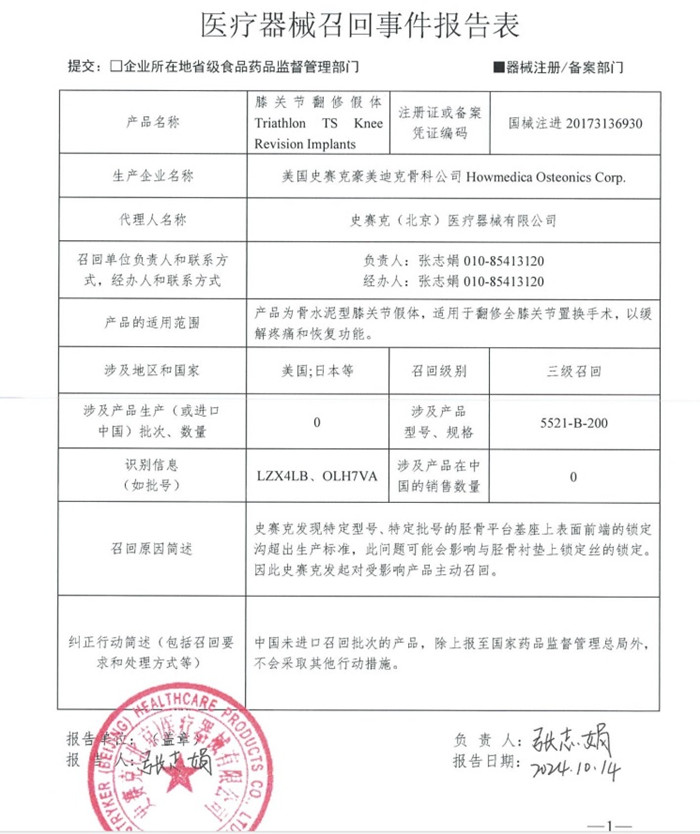
四、美國史賽克豪美迪克骨科公司 Howmedica Osteonics Corp. 對膝關節(jié)翻修假體主動召回
史賽克(北京)醫(yī)療器械有限公司報告,由于發(fā)現(xiàn)脛骨平臺基座上表面前端的鎖定溝超出生產(chǎn)標準,生產(chǎn)商美國史賽克豪美迪克骨科公司 Howmedica Osteonics Corp. 對其生產(chǎn)的膝關節(jié)翻修假體Triathlon TS Knee Revision Implants(國械注進20173136930)主動召回。本次召回涉及的產(chǎn)品未進口至中國,具體型號、規(guī)格及批次等詳細信息見《醫(yī)療器械召回事件報告表》。
五、海奧技術有限公司Hyaltech Ltd.對眼用透明質(zhì)酸鈉主動召回
卡爾蔡司(上海)管理有限公司報告,由于發(fā)現(xiàn)產(chǎn)品泡罩存在破洞缺陷,生產(chǎn)商海奧技術有限公司Hyaltech Ltd.對其生產(chǎn)的眼用透明質(zhì)酸鈉Z-Hyalin Plus Viscoelastic solution for use in intraocular surgery(國械注進20193162441)主動召回。召回級別為二級召回。本次召回涉及產(chǎn)品未進口至中國,具體型號、規(guī)格及批次等詳細信息見《醫(yī)療器械召回事件報告表》。

如有進口醫(yī)療器械注冊代理服務需求,歡迎您隨時方便與杭州證標客醫(yī)藥技術咨詢有限公司聯(lián)絡,聯(lián)系人:葉工,電話:18058734169,微信同。