- 聯系我們

聯系電話:0571-86198618手機: 18058734169 (微信同)手機:18868735317(微信同)周一至周日 8:00~22:00
在線客服周一至周日 8:00~22:00
-
醫療器械注冊人制度最新進展 近日,國務院對北京市繼續開展和全面推進服務業擴大開放綜合試點的請示作出批復,允許北京市醫療器械注冊人委托京津冀地區醫療器械生產企業生產醫療器械”。意味著對醫械行業產生重大影響的醫療器械注冊人制度正式擴展至北京市,所委托的生產企業更是擴展至河北省。 時間:2019-4-8 23:19:13 瀏覽量:2185

-
紹興查處一起醫療器械經營許可企業虛假宣傳案 日前,浙江省紹興市越城區市場監管局以及公安、檢察院等部門,對涉嫌醫療器械虛假宣傳的“金麒麟中心”進行查處,共查處3個體驗分店,抓獲涉案人員10名。 時間:2019-4-8 22:47:15 瀏覽量:2603

-
國家藥監局發布醫療器械臨床試驗指導原則(透明質酸鈉類面部注射填充材料) 隨著科學技術的不斷發展,透明質酸鈉類面部注射填充材料產品日益增多。為了進一步規范該類產品上市前的臨床試驗,并指導該類產品注冊申請人在申請產品注冊時臨床試驗資料的準備,國家藥品監督管理局醫療器械技術審評中心制訂了《透明質酸鈉類面部注射填充材料臨床試驗指導原則》。 時間:2019-4-8 0:00:00 瀏覽量:6099

-
醫療器械經營許可企業為什么要通過GSP認證? 為保障醫療器械產品經營過程中的質量安全,國家要求在醫療器械采購、驗收、貯存、銷售、運輸、售后服務等環節均需符合GSP規定。 時間:2019-4-7 22:37:37 瀏覽量:6217

-
關于發布醫療器械臨床試驗機構條件和備案管理辦法的公告(2017年第145號) 為貫徹落實中共中央辦公廳和國務院辦公廳印發的《關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》和《醫療器械監督管理條例》,落實國務院簡政放權、放管結合、優化服務的精神,深入推進審評審批制度改革,今日(11月24日),國家食品藥品監管總局會同國家衛生計生委聯合發布《醫療器械臨床試驗機構條件和備案管理辦法》,自2018年1月1日起施行。 時間:2019-4-7 0:00:00 瀏覽量:8262

-
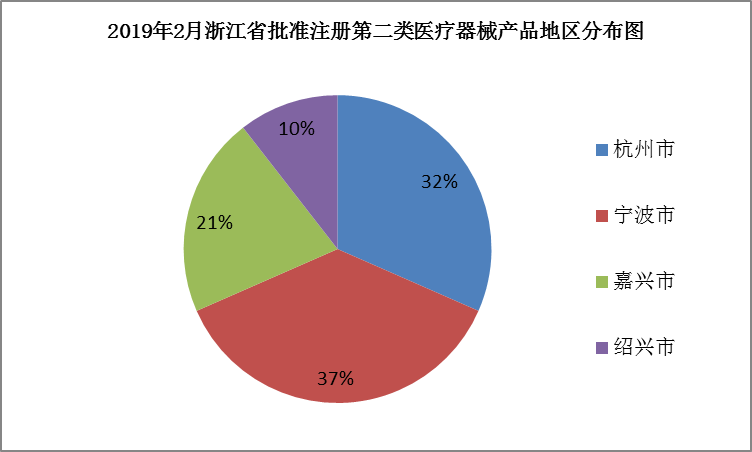
2019年2月浙江省共批準第二類醫療器械注冊產品19個,比上個月24個略微下降 近期,浙江省藥品監督管理局公布2019年2月共批準第二類醫療器械注冊產品19個,比2019年1月批準的第二類醫療器械注冊產品24個略微下降。 時間:2019-4-7 0:00:00 瀏覽量:2558
-
醫療器械臨床試驗管理備案 時間:2019-4-7 0:00:00 瀏覽量:5043

-
醫療器械經營許可企業飛檢需要遵守哪些原則? 隨著人民對生活健康水平要求不斷提高,醫療器械產業蓬勃發展。相應的,對醫療器械的行政監管也提出了更高的要求。在此大背景下,飛行檢查是一個很重要也很有效的措施。醫療器械飛檢能夠有效督促企業加強質量控制,保證生產安全,幫助企業實現規范化、標準化生產和經營。 時間:2019-4-6 0:00:00 瀏覽量:3220

-
紹興企業怎樣辦理醫療器械經營許可證 醫療器械經營許可證是所在地藥監局在審批、監管,浙江省各地醫療器械經營許可證及醫療器械經營備案憑證辦理存在差異,總體而言,紹興市是浙江省監管最嚴格地區之一,辦理流程及要求與浙江省其他地方也存在差異。證標客在此為大家簡要說明。 時間:2019-4-6 22:44:47 瀏覽量:2390

-
境外醫療器械臨床試驗數據用于進口醫療器械注冊申報的指導原則 境外醫療器械臨床試驗數據可以用于進口醫療器械注冊申報,意味著國外大量的醫療器械產品進入中國市場,將大大提速!雖然可能會對本土企業帶來沖擊。但能讓民眾更早地用上更好、更多的醫療器械產品。短期內可能還不會造成什么影響,但從三五年、甚至10年來看,必定對我國醫療器械行業帶來巨大的影響。 時間:2019-4-6 0:00:00 瀏覽量:4524

-
請注意:這些醫療器械注冊證已注銷! 近日,上海市藥品監督管理局公布對上海澳華光電內窺鏡有限公司持有的注冊證編號分別為 “滬食藥監械(準)字2014第2221309號” “滬械注準20162220068” “滬械注準20162220657” 的《醫療器械注冊證》依法予以注銷。 時間:2019-4-6 0:00:00 瀏覽量:3877

-
哪些情況可以不進行醫療器械臨床試驗? FDA認為,一些醫療器械無法或不需要進行大型、盲法、隨機、對照臨床試驗。通常情況下,廣泛的試驗研究、動物研究和模擬研究已經可以證明醫療器械的安全有效性。事實上,FDA還考慮可以接受更大程度的不確定性以加快產品上市,并依靠上市后的臨床數據提供更多的安全有效性驗證資料。對于已在其他國家上市或有其他適應證的醫療器械,來自注冊機構或研究機構的數據也可用于支持上市批準 時間:2019-4-5 0:00:00 瀏覽量:2813

-
北京252個醫療器械注冊產品進入國家創新審評審批序列 為貫徹落實《國務院關于改革藥品醫療器械審評審批制度的意見》和《中央辦公廳國務院辦公廳關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》,各省市正在推進醫療器械審評審批制度改革,加速醫療器械創新發展。 時間:2019-4-5 0:00:00 瀏覽量:2085

-
醫療器械經營許可企業注意:藥監局開展耗材“兩票制”大檢查 2019年醫療器械大檢查來了!從生產到流通全覆蓋,從日常檢查、抽查,到重點領域飛檢相結合,尤其流通領域,還要執行耗材“兩票制”落地執行大檢查! 時間:2019-4-5 0:00:00 瀏覽量:2832

-
華為等名企紛紛入局醫械行業,增擴醫療器械經營許可范圍 在不到兩個月的時間里,多個資本巨頭紛紛入局或者加碼醫療器械行業,增擴醫療器械經營許可范圍,足以看出,我國醫療器械市場的發展潛力。巨頭紛紛跨界大健康尤其是醫療器械領域,一方面顯示出醫療器械行業的前景十分向好;另一方面也可以看出,醫療器械行業的賽道上,越來越多跨界巨頭加入,競爭將更加激烈! 時間:2019-4-4 0:00:00 瀏覽量:2447

-
南昌市第三醫院順利通過醫療器械臨床試驗項目現場核查 近日,江西省藥品審評中心專家檢查組一行5人蒞臨南昌市第三醫院,對該院檢驗科承接的臨床試驗項目進行數據真實性、合規性現場核查。被核查項目及醫院藥物臨床試驗機構得到了檢查組的認可,給出了較好的評價。 時間:2019-4-4 0:00:00 瀏覽量:2800

-
醫療器械注冊電子申報信息系統即將上線,注冊申報效率將大大提高 按照國家藥品監管局關于醫療器械注冊電子申報的工作部署,器審中心組織開展了醫療器械注冊電子申報信息(eRPS)系統的建設工作,系統擬于近期上線。 時間:2019-4-4 0:00:00 瀏覽量:3732

-
怎樣設計醫療器械臨床試驗方案 醫療器械臨床試驗是指在具備相應條件的臨床試驗機構中,對擬申請注冊的醫療器械在正常使用條件下的安全有效性進行確認的過程。臨床試驗是以受試人群(樣本)為觀察對象,觀察試驗器械在正常使用條件下作用于人體的效應或對人體疾病、健康狀態的評價能力,以推斷試驗器械在預期使用人群(總體)中的效應。由于醫療器械的固有特征,其試驗設計有其自身特點。 時間:2019-4-3 22:11:26 瀏覽量:2981

-
金華市醫療器械經營許可證/備案怎樣辦理? 根據醫療器械經營監督管理辦法的相關規定,開辦與醫療器械經營有關的企業,以及開辦第二類、第三類醫療器械經營企業,應當提交相關資料向所在地設區的市級食品藥品監督管理部門提出申請辦理第二類、第三類醫療器械經營許可證。 時間:2019-4-3 0:00:00 瀏覽量:2605

-
國家藥品監督管理局新批準醫療器械注冊產品78個 最近,國家藥品監督管理局發布《關于批準注冊78個醫療器械產品公告(2019年第24號)》,共批準醫療器械注冊產品78個。其中,境內第三類醫療器械注冊產品50個,進口第三類醫療器械注冊產品8個,進口第二類醫療器械注冊產品20個。 時間:2019-4-3 0:00:00 瀏覽量:2931

