醫療器械唯一標識,是指在醫療器械產品或者包裝上附載的,由數字、字母或者符號組成的代碼,用于對醫療器械進行唯一性識別。全球主流醫療器械市場,包括我國將逐步啟用醫療器械唯一性標識系統,實現高風險醫療器械全生命周期追溯和管理。
引言:醫療器械唯一標識,是指在醫療器械產品或者包裝上附載的,由數字、字母或者符號組成的代碼,用于對醫療器械進行唯一性識別。全球主流醫療器械市場,包括我國將逐步啟用醫療器械唯一性標識系統,實現高風險醫療器械全生命周期追溯和管理。
一、什么是醫療器械唯一標識(UDI)?
答:“醫療器械唯一標識,是指在醫療器械產品或者包裝上附載的,由數字、字母或者符號組成的代碼,用于對醫療器械進行唯一性識別。”(《醫療器械唯一標識系統規則》第三條)
“醫療器械唯一標識包括產品標識和生產標識。”(《醫療器械唯一標識系統規則》第七條)
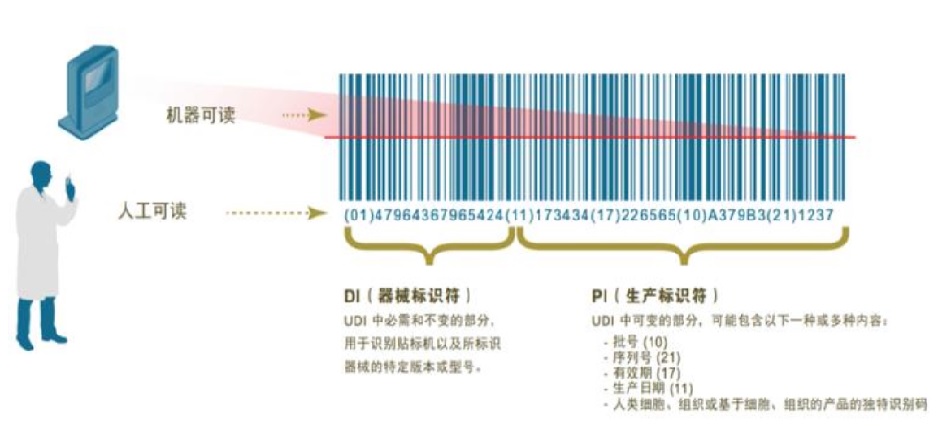
二、UDI中的產品標識(DI)和生產標識(PI)是什么?
答:“產品標識為識別注冊人/備案人、醫療器械型號規格和包裝的唯一代碼;生產標識由醫療器械生產過程相關信息的代碼組成,根據監管和實際應用需求,可包含醫療器械序列號、生產批號、生產日期、失效日期等。”(《醫療器械唯一標識系統規則》第七條)
三、創建、維護和賦予UDI的責任主體是誰?
答:“注冊人/備案人負責按照本規則創建和維護醫療器械唯一標識,在產品或者包裝上賦予醫療器械唯一標識數據載體,上傳相關數據,利用醫療器械唯一標識加強產品全過程管理。”(《醫療器械唯一標識系統規則》第六條)
“注冊人/備案人應當按照醫療器械唯一標識的編制標準創建、維護醫療器械唯一標識。醫療器械唯一標識編制標準應當符合國家藥品監督管理局以及符合本規則要求的發碼機構制定的相關標準。”(《醫療器械唯一標識系統規則》第九條)
四、目前UDI的發碼機構有哪些?
答:目前已在國家藥品監督管理局醫療器械唯一標識數據庫上傳發碼規則的發碼機構有3家,分別為中國物品編碼中心、中關村工信二維碼技術研究院和阿里健康科技(中國)有限公司,有關發碼機構及其規則等信息,請查詢醫療器械唯一標識數據庫官網(https://udi.nmpa.gov.cn/)。
五、UDI數據載體可以采用哪些形式?答:“當前市面上常用的數據載體包括一維碼、二維碼和射頻標簽(RFID)。注冊人/備案人可根據產品的特征、價值、主要應用場景等因素選擇適當的醫療器械唯一標識數據載體。”(《醫療器械唯一標識系統規則》解讀)。
六、什么是醫療器械唯一標識數據庫(UDI數據庫)?答:醫療器械唯一標識數據庫是指儲存醫療器械唯一標識的產品標識與關聯信息的數據庫。(《醫療器械唯一標識系統規則》第三條)
國家藥品監督管理局制定醫療器械唯一標識數據相關標準及規范,組織建立醫療器械唯一標識數據庫,供公眾查詢。(《醫療器械唯一標識系統規則》第十三條)。2019年12月,UDI數據庫系統上線運行(https://udi.nmpa.gov.cn/)。2020年3月,數據庫通過查詢、下載、接口對接三種方式對外提供共享服務。 七、UDI數據庫中的相關數據由誰負責上傳、維護和更新?答:“注冊人/備案人應當按照相關標準或者規范要求上傳、維護和更新唯一標識數據庫中的相關數據,并對數據的真實性、準確性、完整性負責。” (《醫療器械唯一標識系統規則》第十四條)八、注冊人/備案人需要上傳生產標識(PI)信息至UDI數據庫?答:不需要。注冊人/備案人需在數據庫內填報生產標識(PI)是否包含批號、序列號、生產日期、失效日期,具體請查閱UDI數據庫網站首頁的數據申報說明欄目中的數據填報說明(https://udi.nmpa.gov.cn/toDataDocking.html)。
九、哪些包裝層級要求賦予UDI?
答:“注冊人/備案人應當選擇與其創建的醫療器械唯一標識相適應的數據載體標準,對以其名義上市的醫療器械最小銷售單元和更高級別的包裝或者醫療器械產品上賦予唯一標識數據載體,并確保在醫療器械經營使用期間唯一標識數據載體牢固、清晰、可讀。”(《醫療器械唯一標識系統規則》第十二條)
醫療器械唯一標識在哪里申請、醫療器械唯一標識申請網址、醫療器械唯一標識申請條件